大阪大学 2021年 化学 一問一答と解説
2021年 大阪大学 化学の問題から一問一答を作ってみました。
【一問一答】
----↓ 〔1〕 ----
【解答上のポイント】
〔1〕は電池や酸化還元に関する基本的な問題です。問4は難しいですが、他の問題は確実に解答したいところです。
Q-01.
〔1〕問1
化学電池は,正極と負極のそれぞれで進行する[ア]反応と[イ]反応により,化学エネルギーを[ウ]エネルギーに変換する装置である。
リチウム電池は,充電することができない[エ]電池である。
リチウムイオン電池は,繰り返し充放電が可能な[オ]電池である。
[ア]~[オ]にはまる最も適切な語句をそれぞれ記せ。
A-01.
ア: 還元
イ: 酸化
ウ: 電気
エ: 一次
オ: 二次
解説
元々の問題は与えられた語群から適切な語句を選ぶ問題でした。しかし、非常に基本的な内容なので語句が与えれれて
いなくても答えられないといけない問題です。
電池の負極からは電子が出ていきます(負は-で、マイナスの電子と反発して遠くに離れていくイメージ)。
電子が出ていくということは、すなわち酸化です。
電池の正極には電子が入ってきます(正は+で、マイナスの電子を引きつけるイメージ)。電子を受け取るのは還元です。
電池の極につながっている陽極と陰極での反応と混同しないようにしないといけません。
陽極は電池の正極とつながっている電極のことをいいます。電子は正極に向かって流れていきますので陽極では
電子が奪われる反応、すなわち酸化が起こります。
陰極は電池の負極とつながっている電極のことをいいます。陰極は負極から電子が流れ込んできます。
すなわち電子を受け取る反応なので還元反応となります。
また、リチウム電池とリチウムイオン電池の違いに注意が必要です。
Q-02.
〔1〕問2
単体のLiは, LiClを原料として,陽極に黒鉛を,陰極に軟銅(炭素を含む鉄)を用いた溶融塩電解によって得られる。
陽極と陰極で進行する化学変化をそれぞれ電子e-を含むイオン反応式で示せ。
A-02.
陽極: 2Cl- → Cl2 + 2e-
陰極: Li+ + e- → Li
Q-03.
〔1〕問3
単体のLiは,LiCl水溶液の電気分解で得ることはできない。
理由を説明せよ。
A-03.
リチウムはイオン化傾向が大きく、陰極ではリチウムイオンの還元よりも、水の還元が進行するため。
解説
2018年 東京大学 第2問オ にも同様の出題がありました。
「Alの単体は,Al3+を含む水溶液の電気分解では得ることができない。その理由を簡潔に説明せよ。」
Q-04.
〔1〕問4
リチウム電池は,正極活物質にはMnO2,負極活物質には金属Li,電解液には有機溶媒にLi塩を
溶解させた溶液が用いられる電池である。放電により,正極活物質中のMnは4価から3価に変わる。
正極と負極で進行する化学変化をそれぞれ電子e-を含むイオン反応式で示せ。
A-04.
正極: MnO2 + Li+ + e- → LiMnO2
負極: Li → Li+ + e-
解説
正極にLiMnO2ができるとするところが難しいです。
また水は存在しないので反応には現れません。
〔2〕は2種の物質が混合した系における気体の分圧に関する問題です。
通常の問題集に載っていないような問題で、リード文を読んで解答していきます。
問題の設定が複雑なので、状況を理解するのに時間がかかります。分かってしまえば簡単なのですが、 そこまで到達するのに時間がかかってしまうようであれば後回しにしてもよさそうな問題です。
〔2〕は一問一答の題材がないので省略します。
----↑ 〔2〕 ---- ----↓ 〔3〕 ----
〔3〕は有機化学の構造決定の問題です。
基本が分かっていれば、解答できる問題が多いです。
いかに速く正確に解けるかが勝負です。
構造決定の問題を多数こなして、問題に慣れるようにしたいところです。
Q-05.
〔3〕問1
化合物AとBの混合を,乾いた酸素を通しながら酸化銅を用いて完全燃焼させ[ア]の入ったU字管と[イ]の入ったU字管へ順に通した。
[ア]と[イ]にあてはまる最も適切な物質名を書け。
A-05.
[ア] 塩化カルシウム
[イ] ソーダ石灰
解説
頻出問題です。
Q-06.
〔3〕問2
化合物A 34.0 mgを乾いた酸素を通しながら酸化銅を用いて完全燃焼させ、たところ18.0 mgの水と88.0 mgの二酸化炭素が発生した。
化合物Aの分子量が136.0であるとき、分子式を答えよ。
A-06.
C8H8O2
Q-07.
〔3〕問6
二重結合または三重結合を1つもつ分子式C6H10の脂肪族化合物 Hがある。ただし,炭素原子3つや4つからなる環構造はもたない。
化合物Hを硫酸酸性の過マンガン酸カリウム水溶液と十分に反応させると,枝分かれ構造をもたない化合物Iが得られた。フェーリング液に
化合物1を加えても変化は起こらなかった。化合物Iとエチレングリコールを反応させると,高分子化合物Jが得られた。
化合物Hの構造式を書け。
A-07.
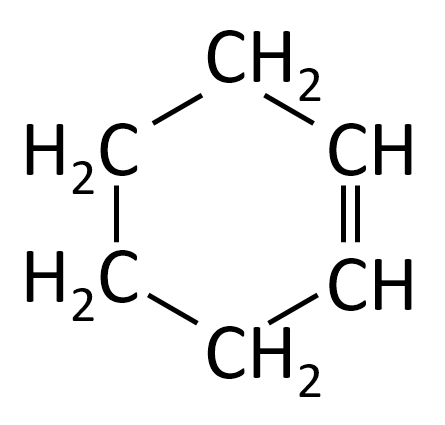
解説
C6H10の不飽和度は2です。すなわち三重結合が1つ、または二重結合が2つ、
または二重結合が1つと環構造が1つ、または環構造が2つ、などが考えられます。
この中で問題文にあてはまるのは「二重結合が1つと環構造が1つ」です。
化合物Hを硫酸酸性の過マンガン酸カリウム水溶液と十分に反応させるというのは、化合物Hを酸化することです。
酸化してできた化合物Iはエチレングリコールと高分子を形成するので、-COOHを2個持つジカルボン酸です。
酸化して-COOHが2個できる化合物は解答のものになります。
オゾン分解はC=Cの間に酸素が入り、C=O、O=Cとなりますが、過マンガン酸カリウムという強力な酸化剤を使用すると、酸化が進んで-COOHができます。
〔4〕Ⅰは天然高分子の問題です。
〔4〕ⅡはDNAの問題です。
問題自体は簡単なものが多いですが、図を書くのに時間がかかります。普段から図を書く練習をしておくしかないと思います。
Q-08.
〔4〕Ⅰ問1
デンプンは, 80℃の熱水に浸けておくと,溶ける部分と溶けない部分に分かれる。溶ける部分は[ア]と呼ばれ,
[イ]の①の炭素に結合したヒドロキシ基と④の炭素に結合したヒドロキシ基で次々と縮合した構造をもつ。[ア]は、らせん構造をとるため,
[ウ]反応により鋭敏に濃青色を呈する。一方, セルロースは[ア]と異なり,[エ]の①と④の炭素に結合したヒドロキシ基で次々と縮合し,直線状になる。
[ア]~[エ]にあてはまる最も適切な物質名を書け。
A-08.
[ア] アミロース
[イ] α-グルコース
[ウ] ヨウ素デンプン
[エ] β-グルコース
Q-09.
〔4〕Ⅰ問3
デンプンは, 80℃の熱水に浸けておくと,溶ける部分と溶けない部分に分かれる。
熱水に溶ける部分と溶けない部分の構造上の違いを説明せよ。
A-09.
熱水に溶けるアミロースは、直鎖状の構造を持つが、熱水に溶けない部分は、枝分れの多い構造を持つ。
Q-10.
〔4〕Ⅱ問5
核酸は,生体内に存在する高分子化合物の一種である。環状構造の塩基(核酸塩基)と[オ]が,
炭素原子数が[カ]個の単糖に結合した物質を[キ]とよび,核酸の繰り返し単位となっている。
[オ]~[キ]にあてはまる最も適切な物質名を書け。
A-10.
[オ] リン酸
[カ] 5
[キ] ヌクレオチド
Q-11.
〔4〕Ⅱ問6
アデニンはチミンと,グアニンはシトシンと水素結合を介して,それぞれ塩基対を形成する。
二重鎖DNA中におけるそれぞれの塩基対の水素結合の様子を示せ。核酸塩基の化学構造は,下図の表記を用いること。なお,下図中のRは単糖を示す。
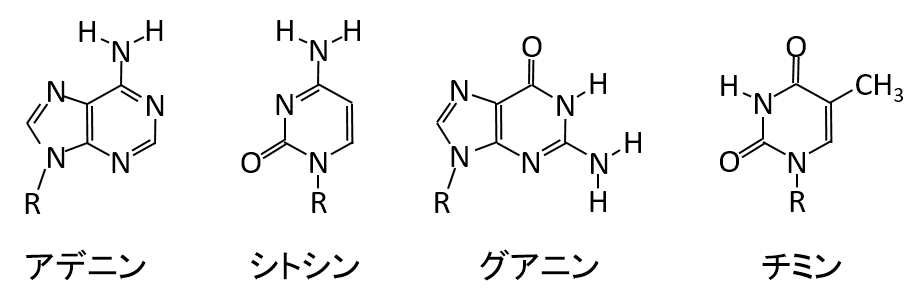
A-11.
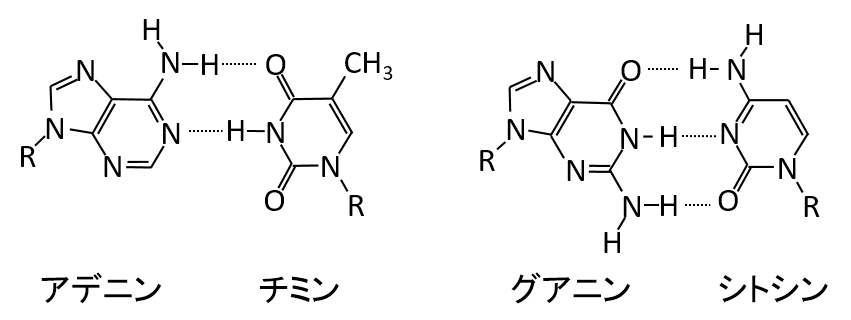
解説
塩基対の水素結合の問題は難易度の高い大学で時々出題されます。
全く何もない状態から塩基対の図を書かせる問題はまず出題されないと思います。
本問のようにある程度ヒントが与えられた状態での出題となると思います。
少なくとも4つの塩基の内どれとどれが塩基対を形成し、その時の水素結合の数が何本かは覚えておく必要があります。
----↑ 〔4〕 ----