2022年 神戸大学 化学 解説
【問題分析】
2022年の神戸大学の化学の問題は、ここ最近の傾向通り、非常に基本的な問題で構成されています。
勉強方法としては教科書と副教材(セミナー化学など)で十分です。
暗記事項と典型的な計算問題ができればすべての問題に対応できます。
差が付きそうなのはⅣです。ⅣはⅠ~Ⅲと異なり少し難しい上に、糖類は最後の方で習うので学習が間に合わなかったという人がいるかもしれません。
試験時間60分で大問は4つです。問題の数はそれなりにあるので解答するスピードも大切です。
【解答上のポイント】
注: このページではすべての問題に対して解答を書いているわけではありません。解答する上で注意すべき問題やポイントとなる点について記載しています。
問題の要点、勉強をする上でのポイントを調べるために読むのが良いと思います。
難問はありません。すべて標準的な問題です。
この手の問題でお決まりの水に溶かしたときに電離しないもの(エチレングリコール)と電離するもの(塩化ナトリウム)が登場します。
まずこの問題で注意すべきは質量モル濃度の定義です。
大学入試において重要な濃度が3つあります。
それは、
1. 質量パーセント濃度 (%): 溶液100g中の溶質の質量(g)
2. モル濃度 (mol/L): 溶液1L中の溶質の物質量(mol)
3. 質量モル濃度 (mol/kg): 溶媒1kgに溶かした溶質の物質量(mol)
です。
上記の内で、沸点上昇や凝固点降下に関係があるのは「3.質量モル濃度 (mol/kg)」です。これは溶媒1kgに溶質が何mol含まれているかで表す濃度です。「1.質量パーセント濃度」と異なり、分母となる溶媒の重量には溶質の重量は含まれません。 したがって問2の計算は下記のようになります。
問2
エチレングリコール(C2H6O2)の分子量は62で、1.86gを100gの水に溶かしたため、質量モル濃度 (mol/kg)は下記の通りになります。
\(\displaystyle \frac{\frac{1.86}{62}\quad (mol)}{0.1\quad (kg)} = 0.300\) mol/L
この問題で注意すべき点がもう一つあります。それは解答する数値について、有効数字の桁数が指定されていることです。問2や問3はきれいに割り切れてしまうため、注意していないと例えば問2の答えを0.3として回答欄に記載しまう可能性があります。部分点がもらえるかどうかわかりませんが、少なくとも減点はされます。
冒頭にも述べたように問題の難易度が標準的なレベルであるため、合格最低点はかなり高いと予想されます。そのような状況の中、指示に従わずに減点されてしまうのはダメージが大きいです。
問3
次の図の中で塩化ナトリウムはTA、TB、TCのどれかという問題です。TA、TB、TCは沸点です。一番温度が低く、沸騰した後は時間が経っても温度が変わっていないことから純水はTAとわかります。
問2と同様に塩化ナトリウム水溶液の沸点上昇度を計算してTB、TCのどちらかを調べます。
ここで注意が必要なのはNaClは100%電離する点です。沸点上昇度を計算するときに使う質量モル濃度は溶液内にある粒子のmol数で計算します。イオンの数はNaClのモル数の2倍になりますので、下記のように2倍して計算しなければなりません。
\(\displaystyle \frac{\frac{1.17}{58.5}\times 2\quad (mol)}{0.1\quad (kg)} = 0.400\) mol/L
エチレングリコールの濃度は0.300mol/Lであったので、NaCl水溶液の方が沸点上昇度は大きくなります。したがって答えはTCとなります。
問4
まずエチレングリコールの沸点上昇度が0.156 Kであることから、下記の式に従いモル沸点上昇Kの値を求めます。
計算するとKの値は0.52になります。
Δt=Km
Δt:沸点上昇度 (K)
K:モル沸点上昇 (K・kg/mol)
m:質量モル濃度 (mol/kg)
Kの値は溶媒に固有の値であるため、求めたKの値を使ってNaCl水溶液の沸点上昇度を求めることができます。この値は0.208となります。
またまたここで注意が必要です。問われているのはNaCl水溶液の沸点上昇度ではなく、TCとTBの温度差です。そしてこの問題でも有効数字の桁数が指定されているので、解答欄に書く答えは0.208-0.156=0.0520 Kとなります。
問5
水溶液BやCの沸点が上昇する理由を答える問題です。これも定番なのでわからない人は必ず覚えてください。
「水が沸騰により蒸発して減ることで溶液の質量モル濃度が増加するため。」
問6
水が蒸発して沸点上昇度が0.260 Kになったときについての問です。
計算方法は色々ありますが、一つの方法としては次のようになります。
まず沸点上昇度が0.260 Kとなる時の濃度を求めます。その値は0.5 mol/kgです(0.260=0.52 × mから、m=0.5)。次に溶質0.04molは変化しないので溶媒の量が何キログラムになったら沸点上昇土が0.260になるか求めます。溶媒の量をM (kg)とすると、
0.04(mol)/ M (kg)=0.5からM=0.08 (kg)=80 (g)
となります。
またまたここで注意が必要です。問われているのは水溶液Cの質量です。
有効数字3桁の指定と合わせて考えると、溶液Cの質量は80 + 1.17 = 81.17 ≒ 81.2 gが答えとなります。
----↑ Ⅰ ----
----↓ Ⅱ ----
Ⅱは無機化学系の問題です。
Ⅰに引き続き標準的な問題です。
まず、Ⅱで問われている知識問題の解答を次に列挙します。
両性金属(両性元素)、アルマイト、テルミット、ボーキサイト、溶融塩電解(融解塩電解)
どれも教科書に載っているものばかりです。わからないものがあれば明らかに知識不足です。
化学で覚えることは相当な量ありますが、試験で良い点数を取るためにはどんどん覚えていくほかありません。
教科書に載っているものはすべて覚えるつもりで頑張りましょう。
問2
問2の中に電極を答える問題があります。答えは陰極であって負極と答えてはいけません。
正極、負極は電池の電極のことで、電気分化するために電池の正極、負極につないだ電極は陽極、陰極といいます。
問6
「電気分解で1.80 gのAlを1時間で析出させるために必要な電流の値(A)」を答える問題があります。
この問題では電気量(C)の定義を知っておかなければなりません。
これも当然知っておくべき内容です。
電気量(C)は次の式で計算されます。
電気量(C) = 電流(A) × 時間(秒)
----↓ Ⅱ ----
Ⅲは有機化学の問題です。
Ⅰ、Ⅱに引き続き標準的な問題です。
問1~6の中で難しいのは問6のみです。難しいといっても絶対わからないというようなものではありません。
イメージとしては問1~5が簡単すぎるのでそれよりも少し難しいという意味です。
問1
「アニリンの希塩酸溶液を氷冷しながら、亜硝酸ナトリウム水溶液を加えると化合物Bが生成した。化合物Bは何か。また、5℃以上で化合物Aと気体分子Cに分解する。気体分子Cは何か」という問題です。
これは教科書に載っている基本事項です。
化合物Bは「塩化ベンゼンジアゾニウム」です。
塩化ベンゼンジアゾニウムは5℃以上でフェノール(化合物A)と窒素に分解します。
したがって、気体分子Cは窒素です。
問2
上記の反応で化合物Bが生成する反応はジアゾ化です。
問3、4
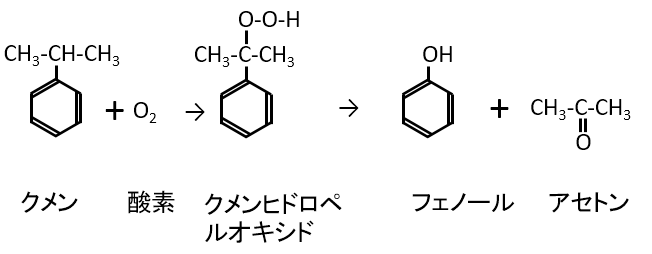
実験2はクメン法を意味しています。クメン法は頻出項目です。
実験2を反応式で表すと次の通りになります。
化合物Dの構造式は下記の反応式のクメンヒドロペルオキシドになります。
クメンヒドロペルオキシドの構造もよく問われますので、必ず覚えましょう。
「クメンヒドロペルオキシドを分解すると化合物Aと化合物Eが生成した」とあります。
他の部分の記述から化合物Aはフェノールであるため、化合物Eはアセトンになります。
問5
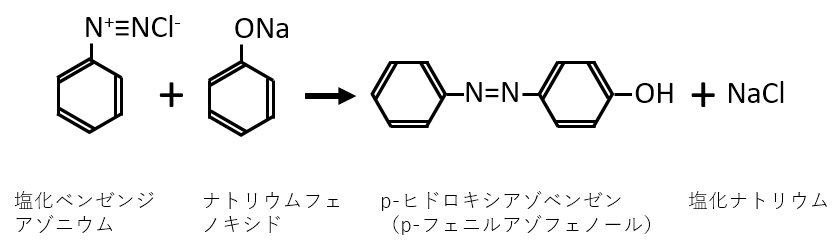
「実験3:化合物A(フェノール)の水酸化ナトリウム水溶液に化合物B(塩化ベンゼンジアゾニウム)の水溶液を加えると、橙赤色の化合物Fが生成した。化合物Fは何か」
という問題です。
これも教科書に載っているもので、基本中の基本です。
問6
問1~5は教科書に載っている基礎事項を答えるだけでしたが、問6は少し考える必要があります。
問6は「分子式C11H12O2で表されるエステルを、水酸化ナトリウム水溶液中で加水分解(けん化)したのち中和すると、カルボン酸と化合物A(フェノール)が生成した。不斉炭素元素を持つカルボン酸の二つの構造異性体を答えよ。」という問題です。
分子式C11H12O2を見ると酸素が2個なのでエステル結合(-COO-)は1個です。
エステル結合1個に水分子1個が反応すると、エステル結合が切れて-COOHと-OHに分かれます。
フェノール以外に生成する化合物をXとすると、反応式は次のようになります。
C11H12O2 + H2O → X + C6H6O(フェノール)
両辺の元素の数が合うようにカルボン酸Xの分子式を計算すると、分子式はC5H8O2となります。
不飽和度を計算すると、
\(\displaystyle \frac{5 \times 2}{2}=1\)
となるため、二重結合が1個あるか環状構造が1個あることがわかります。
不飽和度の計算がわからなければこのサイト内の不飽和度の計算のページを見てください。
飽和不飽和度は水素不足指数ともいいます。水素不足指数の方が実際の状態と合うように思いますね。
例えば二重結合ができると飽和のときには結合している水素2個が不足しているというように考えることができます。
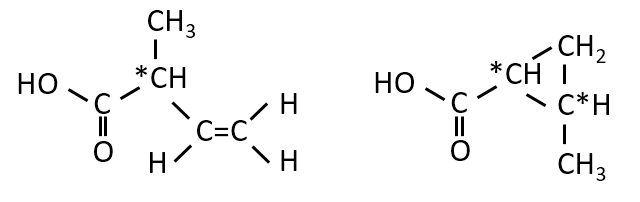
答えは次の二つになります。
環状構造は有機化学の最後の問題の定番の答えです。環状でない構造はまず初めに検討すると思いますが、環状構造も忘れず検討しましょう。
----↓ Ⅱ ----
Ⅳは糖類の問題です。
この問題はⅠ~Ⅲと違い、得点差が付きそうな問題です。
基本という点から外れた問題ではありませんが、「果たしてここまでしっかり勉強しているかどうか」を試した問題といえます。
問1
まず初めに穴埋め問題です。
アは二糖類のスクロースが分解した時、何という単糖ができるか答える問題です。グルコースは問題文に書いてくれていますのでもう一つが何かです。
答えはフルクトースです。
今回問われたのはフルクトースですが、入試で覚えておくべき二糖類は次のものです。
マルトース(麦芽糖)、セロビオース、ラクトース(乳糖)、スクロース(ショ糖)、トレハロース
さらにこれらの二糖類は次のように単糖類に分解することまで覚えておかなければなりません。
マルトース(麦芽糖) → α-グルコース + α-グルコース
セロビオース → β-グルコース + β-グルコース
ラクトース(乳糖) → β-ガラクトース + α-グルコース
スクロース(ショ糖) → α-グルコース + β-フルクトース
トレハロース → α-グルコース + α-グルコース
記憶量の限界を試されているようですが、覚えた分だけ得点につながります。逆にいうと覚えていないと失点する可能性が高くなります。
復習するときは、スクロースがグルコースとフルクトースに分解するということを確認するのはもちろんのこと関連する他の二糖類についてもかくにんすると得点力が上昇します。
問2
問題文にある(i)~(iv)の反応は次の通りです。
(i)還元性を持つものを検出する反応
(ii)枝分れしていないデンプンであるアミロースを検出するヨウ素デンプン反応
(iii)ペプチド結合を2つ以上もつペプチドを検出するビウレット反応
(iv)アミノ酸のアミノ基(-NH2)を検出するニンヒドリン反応
すべて教科書に載っている反応ですが、整理して正確に覚えておく必要があります。
問3
枝分れ構造のデンプンであるアミロペクチンに関する問題です。
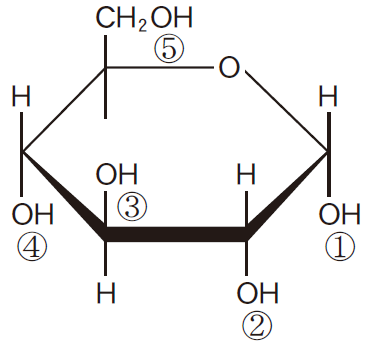
アミロペクチンを構成するグルコースの-OH基の一部は結合に使われるため、場所によって-OH基の数が異なることを問われています。
横につながっている所では下の図で①と④が結合に使われているため、残っている-OH基は②、③、⑤になります。←Aの答え。
主鎖の中で枝分れの起点になっている部分は①、④、⑤が結合に使われるため残っている-OH基は②、③になります。←Bの答え。
問4
アミロペクチンの分枝の数を計算する問題です。
アミロペクチンの構造を模式的に描くと下図のようになります。
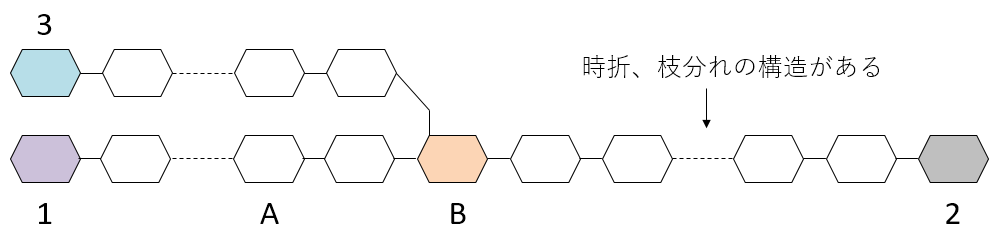
鎖の中にあるAと枝分れの起点になるBのモル数は与えれれているのですが、この問題で難しいのは計算するときに自分で上図の3の数を設定する必要がある点です。3は枝分れの数、すなわちBと同じだけあるので無視することはできません。尚、1と2は分子の端に1個ずつしかないため、無視して計算します。また、1と3は同じものです。
したがって分子全体でグルコースのモル数は
0.24 + 0.012 + 0.012 = 0.264 mol
となります。
0.264 molの中で枝分れの起点になるBの数は0.012 molなので起点の分子の割合は次のようになります。
0.012/0.264
重合度が9.3 × 104、すなわちグルコースの数が9.3 × 104個あるので、枝分れの個数の計算式は次のようになります。
9.3 × 104×0.012/0.264 = 4.23 × 103 ≒ 4.2 × 103
問5
アスパルテームを加水分解すると、下図のXとYの位置で切れます。
Xがペプチド結合、Yがエステル結合です。
二種類のアミノ酸が「あ」と「い」の部分で、メタノールが「う」の部分です。
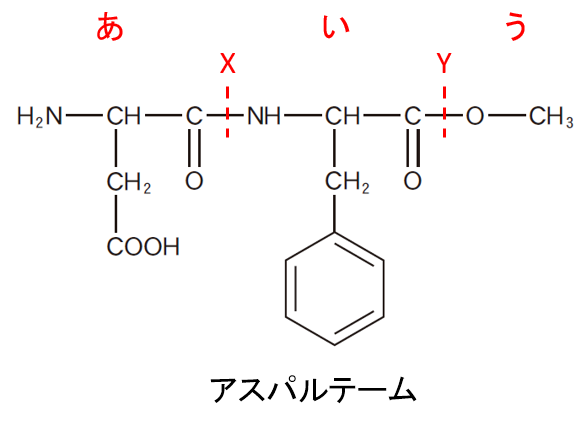
「あ」と「い」のアミノ酸に電圧をかけたとき、中性において、より陽極側に移動する、すなわち負に帯電しているのは-COOHを2個持つ「あ」の部分です。
中性でのイオン化状態で構造式を書かなければならないので、
H2N-の部分はH3+N-
-COOHの部分はCOO-
と描かなければなりません。