2021年 神戸大学 化学 一問一答と解説
2021年の神戸大学の化学の入試問題から一問一答を作ってみました。
2021年の神戸大学の化学の問題は、標準的な問題の間に難しい問題が少し挟み込んであります。
試験時間60分に対して問題が多いため、時間がかかりそうな問題は後回しにして、短時間でできる問題で効率よく点数を積み重ねていく必要があるように思います。
----↓ Ⅰ ----
Ⅰは反応速度と平衡の問題です。
題材は、平衡の問題で定番のH2とI2からHIができる反応です。 リード文が長いため、解答に必要な部分をいかに速く見つけられるかが勝負です。
例えば問1では正反応と逆反応の速度定数を問われていますが、正反応と逆反応では求める方法が異なります。
正反応の速度定数は実験1から求めることができます。逆反応の速度定数も同じように実験2から求められそうですが、別の実験の項目を見なければなりません。
丁寧に読んでいけば、どの問題も解答は可能ですが、ほとんどが計算問題のため速く間違いなく計算していく必要があります。
ただし、どの問題も計算をしやすいように数値が設定されています。
計算問題で難しかったのは問4です。
このタイプの問題では通常[H2]と[I2]の濃度は同じに設定されることが多いですが、本問は[H2]と[I2]の濃度が異なっていました。[H2]と[I2]の濃度が同じだと、両辺の平方根をとることにより一次方程式にできるので簡単に方程式を解くことができるのですが、この問題では[H2]と[I2]の濃度が異なっているので、濃度を求めるために二次方程式を解く必要があります。
二次式を因数分解して二次方程式を解かなければなりませんが、少し複雑な因数分解のため、時間がかかってしまうと後の問題を解答する時間が減ってしまうので要注意です。
Ⅰは一問一答の題材がないので問題は省略します。
----↓ Ⅱ ----
Ⅱは無機化学系の複合問題です。内容は化学反応式と電気分解でした。
ほとんどが基本的な問題でしたが、ヨウ素がヨウ化カリウム水溶液に溶けたときにできるイオン(問4)、塩化ナトリウムを電気分解して塩素を作る工業的製造方法において、水槽を仕切っている膜(問7)を答える問題が難しかったと思われます。
また、塩素のオキソ酸は4種類ありますが、それらすべてを覚えていると、問2の塩素が水に溶けたときにできる物質を答える問題はどれを書くべきか解答に迷ったかもしれません。
塩素が水に溶けてできる物質は、最も酸化力が弱い次亜塩素酸です。それ以外は単に塩素を水に溶かすだけではできません。
Q-01.
問1
フッ素と水との反応の化学反応式を示せ。
A-01.
2F2 + 2H2O → 4HF + O2
Q-02.
問2
塩素の水溶液を塩素水と呼ぶ。
塩素水に存在する物質のうち、最も酸化数が大きい塩素を含むものを物質名で答えよ。また、その物質における塩素の酸化数を答えよ。
A-02.
次亜塩素酸、+1
解説
塩素のオキソ酸は強い順に下記のものがあります。
HClO4 > HClO3 > HClO2 > HClO
過塩素酸 塩素酸 亜塩素酸 次亜塩素酸
塩素を水に通して得られる水溶液を塩素水といいます。
本問は、塩素を水に通して作られる塩素水ですので次亜塩素酸しか存在しません。
(化学重要問題集 2021 1)
Q-03.
問3
臭素の水溶液を臭素水と呼ぶ。
C2H6、C2H4、C2H2の分子式で表される炭化水素のうち、十分量を臭素水に通しても脱色することができない炭化水素をすべて答えなさい。
A-03.
C2H6
解説
二重結合や三重結合をもたないC2H6が正解となります。
問題では「すべて答えなさい」としてあり、紛らわしい問い方ですが、答えは一つしかありません。
Q-04.
問4
ヨウ素は、水には溶けにくいが、ヨウ化カリウム水溶液には新たにイオンを生じて溶ける。
新たに生じるイオンの化学式を答えなさい。
A-04.
I3-
解説
三ヨウ化物イオンI3-が生じて溶液は褐色を呈する。
I2 + I- ⇄ I3-
センター試験2018年 第3問 問2にも同じような問題があります。センター試験でも出題されていますので、基本レベルの問題です。
Q-05.
問5
塩素は、酸化マンガン(Ⅳ)を入れたフラスコに濃塩酸を加え、加熱することにより得られる。
化学反応式を答えよ。
A-05.
MnO2 + 4HCl → MnCl2 + 2H2O + Cl2
Q-06.
問6
塩素は、酸化マンガン(Ⅳ)を入れたフラスコに濃塩酸を加え、加熱することにより得られる。
発生した気体は二つの洗気びんをA、Bを順に通った後に、「ア」置換により捕集される。
A、Bに入れる液体とその理由、および「ア」に入る適切な語句を答えよ。
A-06.
A: 水、塩化水素を除去するため。
B: 濃硫酸、水蒸気を除去するため。
「ア」: 下方
Q-07.
問7、8
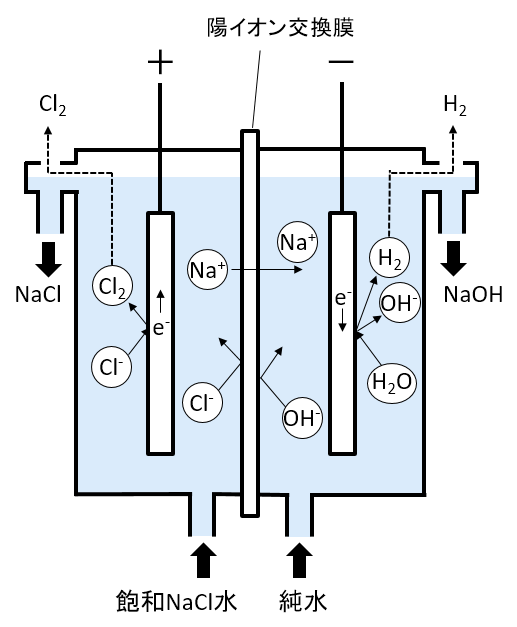
塩素と水酸化ナトリウムを同時に作る工業的方法について、図を書いて説明せよ。
A-07.
陽イオン交換膜で仕切られた水槽の陽極側にNaCl、陰極側に水を入れて電気分解する。NaCl水と純水を連続的に供給して、Cl2とNaOHを連続的に作る。
この製造方法はイオン交換膜法という。
Q-08.
問7、8
塩化ナトリウムを電気分解したとき、陰極と陽極で起こる変化を、それぞれ電子e - を含むイオン反応式で答えよ。
A-08.
陰極: 2H2O + 2e- → H2 + 2OH-
陽極: 2Cl- → Cl2 + 2e-
----↓ Ⅲ ----
Ⅲは有機化合物の構造決定の問題です。
構造決定で定番のオゾン分解が題材として使われています。オゾン分解は高校で習わないため、本問でも解説がついていますが、いろいろな大学で頻出ですので、リード文を見て理解するのではなく、あらかじめ反応の機構を覚えておく必要があります。
この問題は、反応の条件設定が複雑で、有機化合物中のC、H、Oの比を計算したり、条件整理をしたりする必要があるので、かなり時間がかかってしまう印象です。
今年の問題は全体的に時間がかかるものが多いので、簡単にできる問題を素早く見分けて解答し、時間がかかりそうなものは後回しにするのがよいかもしれません。
例えば、Ⅲの問題の問1はヨードホルムの分子式を書けという問題です。また、問2は還元性を示す官能基を答える問題です。こういう問題はじっくり読んで考える必要がないので、Ⅲを解答しないとしても、問1と2だけは解答しておきたいです。
Q-09.
問1
ヨードホルムの分子式を書きなさい。
A-09.
CHI3
Q-10.
問2
有機化合物をアンモニア性硝酸銀水溶液に加えて温めると、銀が析出するとき何という官能基を持つか答えよ。
A-10.
ホルミル基(アルデヒド基)
----↓ Ⅳ ----
Ⅳはペプチドのアミノ酸の配列を答える問題です。
ペプチドのアミノ酸の配列を答える問題は入試の定番問題の一つですが、解答する練習をしておかないと、正解するのは難しいです。
アミノ酸の配列は順番があるため、例えばAとBのアミノ酸からなるペプチドはABとBAの二種類が考えられ、同じものではないことに注意が必要です。
なぜこのような違いが出るかというと、ペプチドはアミノ酸のアミノ基とカルボキシ基が結合してできますが、上記の例で、Aが結合にアミノ基を使うか、カルボキシ基を使うかの2パターンが考えられるためです。
Q-11.
問1 ア
ペプチドに酢酸鉛(Ⅱ)を加えて黒色沈殿ができるとき、何の元素が含まれているか答えよ。
A-11.
S、硫黄
Q-12.
問1 イ、ウ
ペプチドに濃硝酸を加えて加熱すると黄色になるとき、何がどうなるか答えよ。
A-12.
ベンゼン環がニトロ化される
Q-13.
問1 イ、ウ
ペプチドの水溶液に水酸化ナトリウムを加え、さらに少量の硫酸銅(Ⅱ)水溶液を加えたところ赤紫色に発色した時、何がわかるか答えよ。
A-13.
ペプチドがトリペプチド(アミノ酸が3個結合した化合物)以上