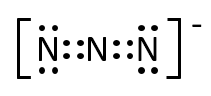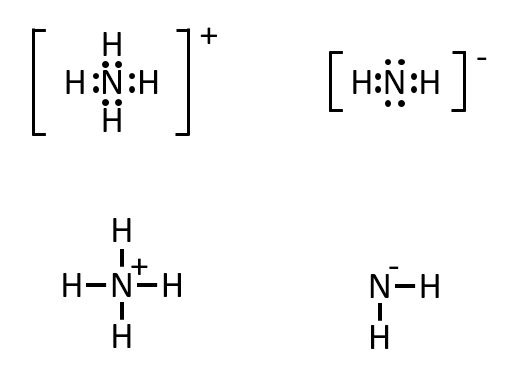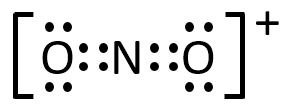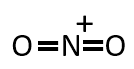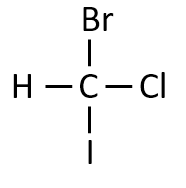【問題分析】
東京医科歯科大学の化学は高校の範囲を超えた問題が多く出題されています。そのため、大学入試の範囲の問題を着実に解答し、高校の内容を超えたものでどれだけ点数が取れるかの勝負という感じがします。
2021年の大問1~3の中で一番難しいのは1です。高校では習わない形式電荷や自己解離という内容で、おそらく初めて見るような問題だと思います。
大問1の問1~4まではリード文をよく読めばできなくはない問題です。リード文を読んですぐに内容が理解できるかどうかですね。
大問1の問5のギ酸の自己解離に関する計算問題はかなり面倒です。また1の問6(2)は高校の内容を逸脱していますので正答率は低いのではないでしょうか。
大問2と3はところどころに難しい問題がありますが、1よりははるかに解答しやすいと思います。
化学に割ける時間が60分で短時間勝負ということを考えると、大問1は避けて、大問2または3から始める方が点数を取りやすいと思います。
2021年の東京医科歯科大学の化学の入試問題から一問一答を作ってみました。
—-↓ 問題1 —-
【解答上のポイント】
問題1は大ざっぱにいうと高校の内容を超えた無機化学や有機化学の問題です。
電子式と形式電荷、自己解離と自己解離で生じたギ酸イオンの割合計算、ニトロベンゼンができるときの化学反応の素過程に関する問題です。
電子式に関しても、通常出題される第2周期の炭素、窒素、酸素ではなく、第3周期の硫黄に関する電子式が出題されています。
リード文を読めばできなくはない問題もありますので、大問1から解き始めるかどうか迷うところです。しかしながら、取り組みやすさを見ると、大問2または3から始めるのがいいと思います。
【一問一答】
Q. 問1
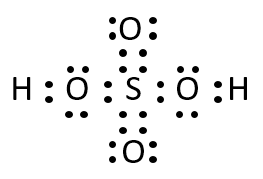
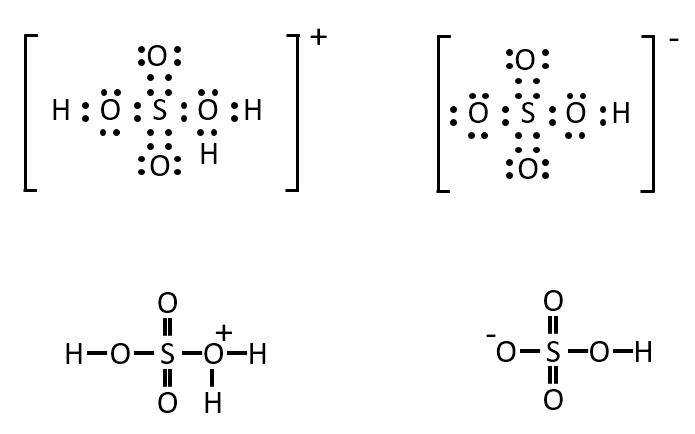
硫酸の構造式は下記の通りである。硫酸の電子式を記せ。
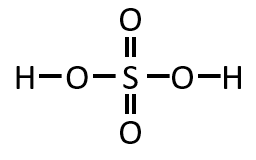
Q. 問3
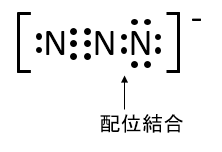
アジ化物イオン(N3–)の構造はオクテット則を満たすものとして、二重結合2個で記すものと、単結合1個、三重結合1個で記すものそれぞれの電子式を示せ。
Q. 問5
溶媒分子同士がH+の授受をしてイオン化することを自己解離という。例えば水の自己解離は下記の通りである。
2H2O ⇄ H3O+ + OH–
アンモニア、硫酸について、それぞれ自己解離の平衡式を書き、生成したイオンの電子式と構造式を記せ。
Q. 問6
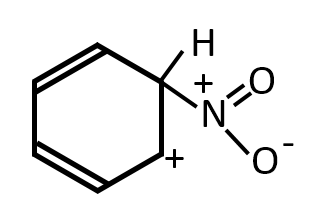
ベンゼンのニトロ化では、混酸中でニトロニウムイオンが生じ(反応a)、これがベンゼン環の炭素原子のうち1個と共有結合で結びつき、不安定な中間体である炭素陽イオンをつくる(反応b)。
HNO3 + 2H2SO4 ⇄ H3O+ + 2HSO4– + ( A )(反応a)
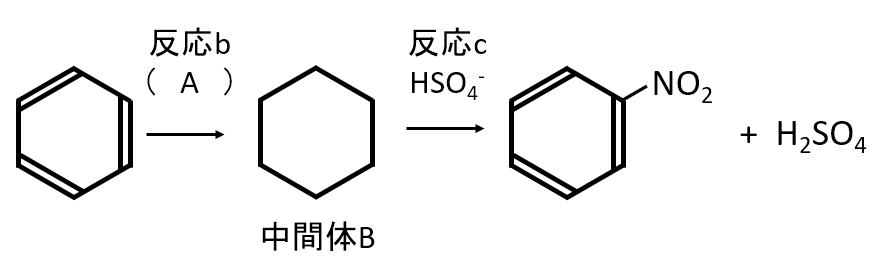
(1) 空欄Aのイオンの電子式と構造式を記せ。
(2) 中間体Bの構造式を完成せよ。
(3) 硫酸はどのような働きをしているか。
—-↑ 問題1 —-
—-↓ 問題2 —-
問題2は無機化学に関する出題です。
問1は定番のリード文中の穴埋め問題です。一見簡単そうですが、答える語句はかなり難易度が高いものです。
周期表も1~20番までではなく、第4周期の遷移金属まで覚えておかなければなりません。
問2のFe2O3の還元の反応式は非常に簡単ですが、問4の接触法の反応式は3段階の反応を覚えておかなければならないので、非常に難しいです。知識の深さが問われます。
問5は鉛蓄電池と比較したときのレドックスフロー電池の利点を答える問題ですが、非常に難しいと思います。
問7の計算問題は最大の謎問題です。何クーロンの電気量を取り出せるかを計算する問題ですが、計算が簡単すぎるので、合っているのか心配になる問題です。
受験生の柔軟性を試そうとしているのでしょうか。
問題2では比較的簡単な問題もありますが、高得点を取るためには非常に深い知識が必要とされます。
Q. 問1 A
トタンは鋼に何をメッキしたものか。
Q. 問1 B
ステンレス鋼に含まれる金属で6族の元素は何か。
Q. 問1 D
7族の元素で+2、+4、+7など多様な酸化物の化合物をつくり、酸化数+4の酸化物は乾電池の正極や、触媒などに用いられる元素は何か。
Q. 問1 E
単体のバナジウムは、酸化バナジウムにアルミニウム粉末を混合・加熱して製造される。
このような反応を何というか。
Q. 問1 F
硫酸の製造過程で用いられる酸化バナジウムの酸化数を答えよ。
Q. 問2
一酸化炭素でFe2O3を還元して単体の鉄を得る反応の反応式を記せ。
Q. 問3
トタンは屋外で使用されるため、しばしばめっき層に傷がついて、内部の鋼が露出する。その場合に鋼がさびから守られる仕組みをイオン化傾向に基づいて60字以内で説明せよ。
Q. 問4
硫酸の製造過程で酸化バナジウムを使う反応の反応式を記せ。
全体の圧力を上げた場合に、この反応の平衡はどうなるか説明せよ。
Q. 問6
VO2+、VO2+イオンにおけるバナジウムの酸化数はそれぞれいくらか。
—-↑ 問題2 —-
—-↓ 問題3 —-
問題3は有機化学の問題です。
有機化学系のいろいろな集合問題となっています。
医学部の単科大学では有機化学の定番である構造決定の問題が出題されないことが多く、本問題もその傾向を踏襲しています。
「ホルムアルデヒドを約37%含んだ水溶液を何というか」など医学部的な要素を含んだ問題が出題されています。
問6の有機化合物の構造を答える問題は難しかったと思いますが、それ以外は標準的な問題といえます。
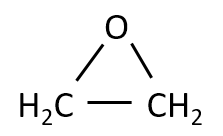
問1は分子式C2H4Oのエチレンオキサイドの構造を書く問題でした。有機の問題の解き方の定番として、分子式が与えられたらまず不飽和度を計算します。
C2H4Oの場合、不飽和度は1なのでC=Cが一つあるか、または環状構造が一つある可能性があります。しかし、問題文では単結合しかないと書いてあるので環状構造があることになります。
Q. 問1
エチレンオキサイドは原子同士が単結合のみで結合しており、その分子式はC2H4Oである。その構造式を記せ。
Q. 問2
エチレンオキサイド(CH2OCH2)を無毒化する方法において、
(1)完全燃焼する方法
(2)水と反応させてエチレングリコール(1,2-エタンジオール)にする方法
がある。
(1)と(2)の反応式をそれぞれ記せ。
Q. 問3
トリハロメタン類はCHX3(X:ハロゲン原子)と表される。
(1) 分子内のX1~X3がCl、Br、Iのいずれかである場合、トリハロメタン類の構造異性体は全部で何種類あるか。
(2)光学異性体を持つものの構造式をすべて記せ。
Q. 問4
ホルムアルデヒドを約37%含んだ水溶液を何というか。
Q. 問6
フェノールの工業的製造方法を何というか。
—-↑ 問題3 —-